Anvisa vai avaliar autorização para testes de vacina desenvolvida em MG
31 julho 2021 às 14h42

COMPARTILHAR
Expectativa é de que o imunizante idealizado por pesquisadores da Federal de Minas Gerais esteja disponível para 2022 e possa ser usado com reforço
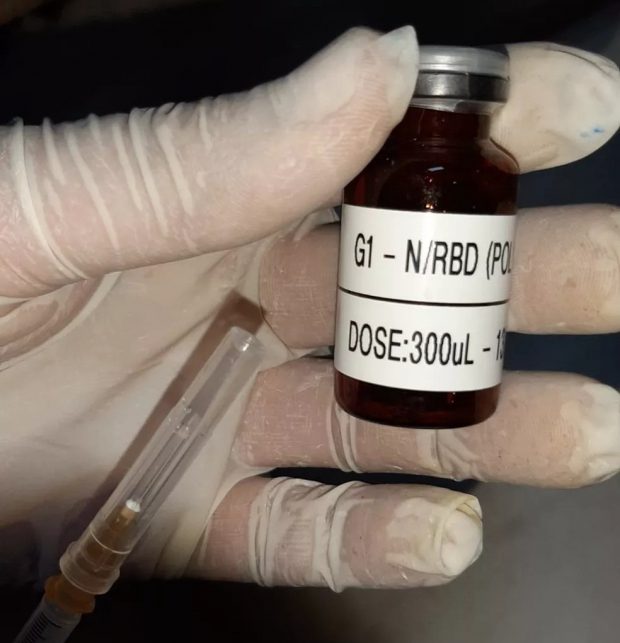
A Spintec, vacina contra a Covid-19, que está sendo desenvolvida por pesquisadores da Universidade Federal de Minas Gerais (UFMG), aguarda autorização da Agência Nacional de Vigilância Sanitária (Anvisa), para o início dos testes em humanos. A solicitação para a realização das fases 1 e 2 do estudo clínico foi enviada nesta sexta-feira, 30.
Previstas para setembro, as duas fases serão desenvolvidas concomitantemente. A primeira, a ser realizada com cerca de 40 voluntários, tem o objetivo de avaliar a segurança da vacina, para identificar se ela provoca ou não efeitos adversos. Já a fase 2, vai reunir 150 a 300 voluntários, e busca comprovar a capacidade de induzir a geração de anticorpos e células de defesa específicas contra o coronavírus.
Para os testes, devem ser convocados voluntários que já tiverem recebido duas doses da vacina Coronavac há pelo menos seis meses. A ideia é avaliar a capacidade de resposta imunológica do organismo à terceira dose de um imunizante.
O objetivo é que a vacina reforce a imunidade das pessoas. Com isso, a expectativa é que a Spintec esteja disponível em 2022, quando toda a população já tiver recebido duas doses do imunizante.
Spintec
Um dossiê foi entregue à Anvisa, com dados e informações sobre o desempenho da Spintec contra a Covid-19 nos testes pré-clínicos realizados em camundongos humanizados. Segundo a UFMG, os resultados foram positivos.
Com isso, a vacina não gerou efeitos colaterais adversos detectáveis e demonstrou a capacidade de produção de anticorpos tanto para proteína S, na qual ocorre a maioria das mutações do coronavírus, quanto para a N. Além disso, foram identificadas respostas protetoras de linfócitos T.
*Com informações do G1