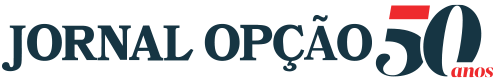Anvisa autoriza testes de aplicação da vacina brasileira desenvolvida pelo Butantan
07 julho 2021 às 20h14
COMPARTILHAR
A fase de testes da Butanvac deve envolver até 6.000 voluntários

A Agência Nacional de Vigilância Sanitária (Anvisa), anunciou nesta quarta-feira, 07, que a vacina desenvolvida pelo Instituto Butantan para combater o Covid-19, a Butanvac, poderá iniciar sua fase de teste. Com isso, as vacinas serão aplicadas em voluntários em duas doses com um intervalo de 28 dias.
As fases 1 e 2 do estudo serão realizadas no Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo (HCFMUSP) e no Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto (HCFMRP) e contarão com até 6.000 voluntários, sendo 418 pessoas apenas para a primeira fase de testes.
Após a fase de aplicação dessas vacinas, o estudo irá observar como o corpo desses voluntários reage a imunidade recebida pela vacina. Essa observação terá como base a comparação com outras vacinas do Covid-19. Além disso, também será analisado se a Butanvac consegue proteger os imunizados contra as novas variantes do SARS-CoV-2. Passado essas fases, o Butantan poderá solicitar a aprovação da Anvisa para o uso da vacina na população geral se o imunizante apresentar eficácia mínima de 50%, como é exigido pela Organização Mundial da Saúde.