Como novos medicamentos são testados em humanos
10 maio 2020 às 00h00

COMPARTILHAR
Quando as esperanças do mundo todo de retornar à normalidade dependem de vacinas ou medicamentos, é importante compreender a forma como os tratamentos são desenvolvidos
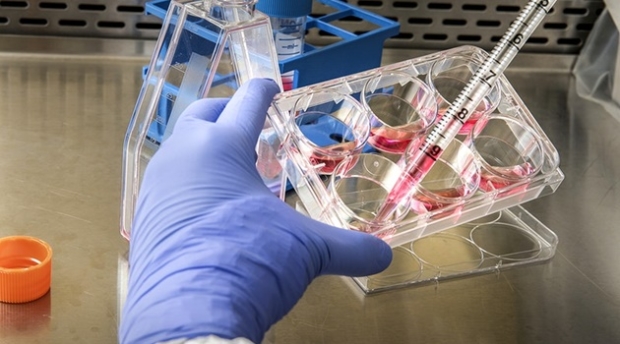
O principal debate dos últimos tempos – como a humanidade vai lidar com um vírus letal e continuar funcionando com o mínimo de sofrimento possível – pressupõe que algum tipo de proteção possa ser desenvolvida contra o novo coronavírus (Sars-CoV-2). Adotar a quarentena até que vacinas ou tratamentos sejam desenvolvidos pela ciência farmacêutica, como fizeram líderes de todo o mundo, é uma forma de comprar tempo para esses cientistas trabalharem em uma solução.
O tempo necessário para o desenvolvimento de um tratamento é longo, mas o método que pode nos dar a solução para a Covid-19 é o mesmo que superou outras pandemias mortais, como a gripe espanhola e seus 50 milhões de mortos. Apostar na imunidade adquirida pelo corpo após exposição com a doença pode apresentar um custo alto demais, já que 20% dos doentes precisam de cuidados médicos e 5% são internados em UTI. Além disso, nada garante que alguém que já foi infectado pelo Sars-CoV-2 não vá desenvolver a doença novamente em caso de reinfecção.
Na realidade, outras vírus da família dos coronavírus (Coronaviridae), como o causador da Mers-CoV de 2003, continua representando um problema para a região onde surgiu. Pesquisadores descobriram que, na Jordânia, 89% das pessoas ainda apresentavam um sistema imunológico apto a responder a reinfecção após 24 meses de contraírem o Mers. Entretanto, o número de pessoas com memória imunológica cai para duas a cada 23 após seis anos da infecção.
Isso quer dizer que deixar o vírus correr livremente entre a população, além de sobrecarregar o sistema de saúde, pode não lograr êxito. Na imprensa internacional, os quatro líderes mundiais que optaram por essa estratégia de enfrentamento do novo coronavírus são chamados de “the ostrich alliance”, ou “a aliança do avestruz”, animal popularmente conhecido por enfiar a cabeça em buracos para não perceber o perigo se aproximando. Estes são o presidente do Brasil e os ditadores do Turcomenistão, Nicarágua e Bielorrússia.
Como são feitos os testes clínicos
A saída mais garantida, portanto, parece ser também a mais difícil. Para assegurar a eficiência e a segurança, o desenvolvimento de vacinas e medicamentos obedece a diversas etapas e procedimentos. Primeiro, para se estudar clinicamente um fármaco, ele já deverá ter sido aprovado em testes pré-clínicos – pesquisa de fármacos inéditos passam por pesquisas in vitro (cultura de células em laboratório), depois in vivo (em animais) e só depois em seres humanos.

Indústrias farmacêuticas que desenvolvem novas fórmulas devem contratar centros de pesquisa independentes que farão a auditoria da pesquisa e fiscalizarão o desenvolvimento do fármaco nesta etapa pré-clínica. Estas empresas enviarão os detalhes verificados no processo a Comissão Nacional de Ética em Pesquisa (Conep). Caso o Conep julgue que o medicamento poderá começar a ser administrado a humanos, se iniciam então os exames em seres humanos, chamados de testes clínicos.
O Instituto de Ciências Farmacêuticas (ICF) é o maior centro de bioequivalência da América Latina e uma das principais instituições a realizar todas as etapas da pesquisa clínica. O Jornal Opção ouviu o endocrinologista Sérgio Vêncio, que conduz estudos no ICF para desenvolvimento de medicamentos e para estudos de bioequivalência.
Sobre os ensaios científicos conduzidos com seres humanos, Sérgio Vêncio explica: “O ICF estuda novas substâncias desenvolvidas por indústrias farmacêuticas e pesquisa suas próprias medicações, desenvolvidas do zero por nós mesmos. Temos, por exemplo, um anti-inflamatório elaborado a partir da casca da jabuticaba que, caso se mostre eficiente e seguro, poderá ir às farmácias. Mas, na maioria das vezes, indústrias farmacêuticas desenvolvem fórmulas e contratam o ICF para estudá-las”.
O ICF possui o único hospital do Brasil dedicado exclusivamente a estudos clínicos, localizado em Aparecida de Goiânia. Por meio do “Eu Ajudo a Ciência”, um banco de voluntários é formado – estas pessoas são remuneradas e recebem consultas médicas e exames laboratoriais gratuitamente. O objetivo é formar um banco com voluntários saudáveis e também com voluntários que sofrem de diversas condições clínicas que podem ser tratadas com novos medicamentos.
“Tanto voluntários saudáveis quanto pacientes que sofrem de alguma condição são sempre informados acerca dos fármacos que estarão experimentando. Ligamos para eles, falamos da pesquisa e os que se interessam vão até o ICF. Lá, discutimos o que é o produto, eles leem o estudo, explicamos riscos e benefícios. Se quiserem, assinam um termo de ciência e, se forem compatíveis com o estudo – o que acontece apenas 50% das vezes, pois os critérios são muito rigorosos – eles serão acompanhados enquanto analisamos os efeitos do medicamento”, explica Sérgio Vêncio.
Portanto, caso você queira montar sua indústria farmacêutica para vender paracetamol, Sérgio Vêncio exemplifica: “Você deve ir à Agência Nacional de Vigilância Sanitária (Anvisa) e obter um exemplar do melhor paracetamol, chamado padrão-ouro. Através do ICF você pode testar sua versão do produto e comparar os resultados com a variante do padrão-ouro, e comparar também os resultados com os de um grupo controle, de voluntários que tomarão apenas um placebo”.

Os estudos clínicos são divididos em quatro fases com número progressivo de sujeitos. O processo, no total, pode levar até dois anos. O objetivo é testar com segurança a biodisponibilidade do remédio – isto é, a quantidade e velocidade na qual o princípio ativo é absorvido, tornando-se disponível para a sua atuação no sítio de ação alvo.
A Faculdade de Ciências Médicas da Universidade Estadual de Campinas (Unicamp) explica as quatro fases dos testes clínicos.
“Na Fase I”, o medicamento é usado pela primeira vez em um ser humano, geralmente um indivíduo saudável e que não tem a doença para a qual o medicamento está sendo estudado. Nesta fase serão avaliadas diferentes vias de administração e diferentes doses, realizando-se testes iniciais de segurança e de interação com outras drogas ou álcool. Cerca de 20 a 100 indivíduos participam dessa fase.
Na “Fase II”, cerca de 100 a 300 indivíduos que têm a doença ou condição para a qual o procedimento está sendo estudado participam desta fase, que tem como objetivo obter mais dados de segurança e começar a avaliar a eficácia do novo medicamento ou procedimento. Diferentes dosagens assim como diferentes indicações do novo medicamento também são avaliadas nesta fase.
Na “Fase III”, depois de concluído o estudo piloto, grandes estudos multicêntricos acompanham milhares de pacientes, de 5 a 10 mil. Em geral, testes são comparados a outros tratamentos existentes e recomendados para o mesmo problema. Durante esta fase se espera obter maiores informações sobre segurança, eficácia e interação de drogas.
Ao participar de uma pesquisa em fase III, o voluntário poderá receber ou o novo tratamento ou o tratamento habitual (ou placebo). Recebendo o tratamento habitual, o paciente será tratado com o que os especialistas avaliam como o melhor tratamento da atualidade. Se o paciente receber o novo tratamento, será tratado com uma alternativa de tratamento que os especialistas esperam obter vantagens significativas sobre o habitual. O objetivo desta fase de estudo é comparar ambos os tratamentos e estabelecer a superioridade de um sobre o outro. Os testes de fase III devem fornecer todas as informações necessárias para a elaboração do rótulo e da bula do medicamento. A análise dos dados obtidos na fase III pode levar ao registro e aprovação para uso comercial do novo medicamento ou procedimento, pelas autoridades sanitárias.
Na fase IV, após um medicamento ou procedimento diagnóstico ou terapêutico ser aprovado e levado ao mercado, testes de acompanhamento de seu uso são elaborados e implementados em milhares de pessoas, possibilitando o conhecimento de detalhes adicionais sobre a segurança e a eficácia do produto. Um dos objetivos importantes dos estudos fase IV é detectar e definir efeitos colaterais previamente desconhecidos ou incompletamente qualificados, assim como os fatores de risco relacionados. Esta fase é conhecida como Farmacovigilância.